Wyroby medyczne
Obecnie firmy produkujące urządzenia medyczne stoją w obliczu stale zmieniających się przepisów, takich jak przepisy unijne dotyczące systemów UDI FDA i systemów MDR, a także konieczności kontrolowania kosztów i skalowania operacji. Etykietowanie i zarządzanie grafiką odgrywają kluczową rolę w sprostaniu tym wyzwaniom.
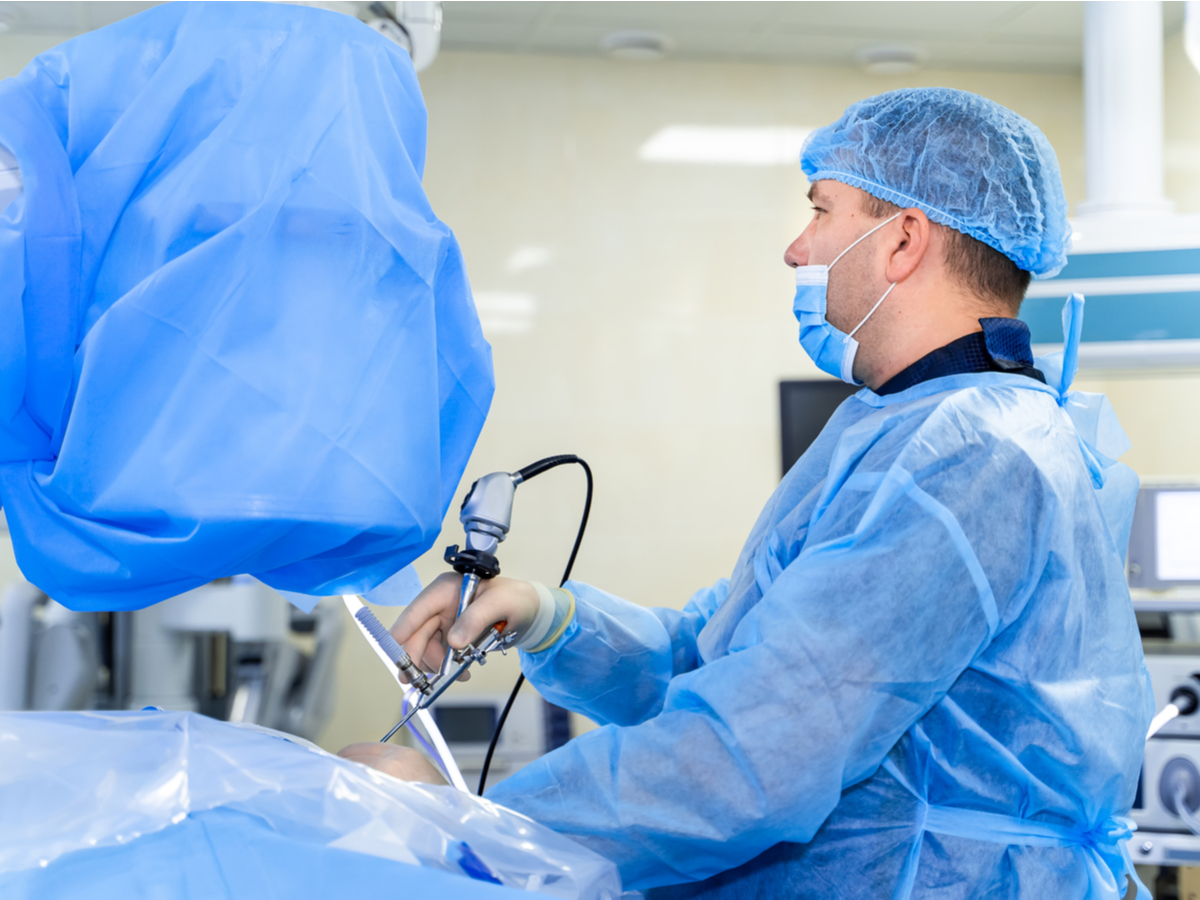





























Utrzymuj dobry stan swojego systemu etykietowania.
Zapewnij zgodność z przepisami
Uproszczony proces zachowania zgodności Potrzebujesz rozwiązania gotowego do walidacji z wbudowanym dostępem opartym na rolach, wersjonowaniem dokumentów, konfigurowalnymi przepływami pracy w zakresie zatwierdzania oraz zapisami elektronicznymi i podpisami elektronicznymi (ERES); wszystko zaprojektowane z myślą o ułatwieniu przestrzegania przepisów.
Zintegruj rzetelne źródła
Bezpieczne dane UDI DI i PI. Unikaj niepotrzebnego ryzyka, gdy pozyskujesz dane z zatwierdzonych systemów zarządzania treścią, zaufanych systemów ERP i innych aplikacji generujących numery seryjne i inne dane potrzebne do spełnienia wymagań prawnych.
Scentralizuj swoje dane
Pełna widoczność. Twoja firma może posiadać wiele lokalizacji, ale to nie znaczy, że powinna być „każdym podmiotem dla siebie”. Scentralizowane etykietowanie zapewnia widoczność i kontrolę oraz możliwość wykazania zgodności i spełnienia standardów korporacyjnych.
Aktywuj zmiany etykiet
Odciąż dział IT. Użytkownicy biznesowi powinni mieć możliwość tworzenia etykiet z medycznymi kodami kreskowymi i zarządzania nimi oraz konfigurowania reguł biznesowych bez wzywania do pomocy działu IT. Dzięki temu mogą szybciej reagować na zmieniające się przepisy.
Zapewnienie bezpieczeństwa/audytowalności
Bezpieczne i solidne dane. Analiza biznesowa oraz pełne możliwości audytu i raportowania umożliwiają monitorowanie i śledzenie wszystkich działań związanych z etykietowaniem oraz funkcji podpisów elektronicznych, dzięki czemu można bezpiecznie przestrzegać przepisów.
Przeanalizuj ponownie starsze systemy
Automatyzacja zapewniająca ułatwienia. Arkusze kalkulacyjne i inne ręczne procesy nie są bezpieczne. Zautomatyzowane, zatwierdzone rozwiązania w zakresie etykietowania umożliwiają łatwe dostosowanie się do nowych wymagań, zabezpieczenie przed przyszłymi przepisami i łatwe skalowanie.
Powiązane zasoby
E-book
6 critical questions and answers on medical device labeling
This Q&A addresses key challenges that medical device companies face and how leveraging innovation in cloud labeling helps organizations succeed in a highly regulated, highly competitive global marketplace.
Webinarium
2024 Top 5 Trends in Labeling and Packaging Artwork Webinar
Watch the Top 5 Trends in Labeling & Packaging Artwork webinar to explore supply chain complexity increases, how cloud becomes a cornerstone of digital transformation and more.
Raport
5 głównych trendów w grafice etykietowania i pakowania w roku 2024
Download this year’s Top 5 Trends in Labeling & Packaging Artwork report to discover why a commitment to bolstering digital transformation strategies through investment in innovative technologies will be critical to fortify supply chains against both current and future uncertainties. You’ll also find out how the supply chain continues to impact today’s businesses and why there is an increased focus on sustainability, digital traceability, automation, and more.