Medizinprodukte
Die heutigen Medizinprodukteunternehmen sehen sich mit sich ständig ändernden Vorschriften wie dem UDI-System der FDA und dem MDR-System der EU konfrontiert, während sie gleichzeitig ihre Kosten kontrollieren und ihren Betrieb skalieren müssen. Etikettierung und Artwork Management spielen eine Schlüsselrolle bei der Bewältigung dieser Herausforderungen.
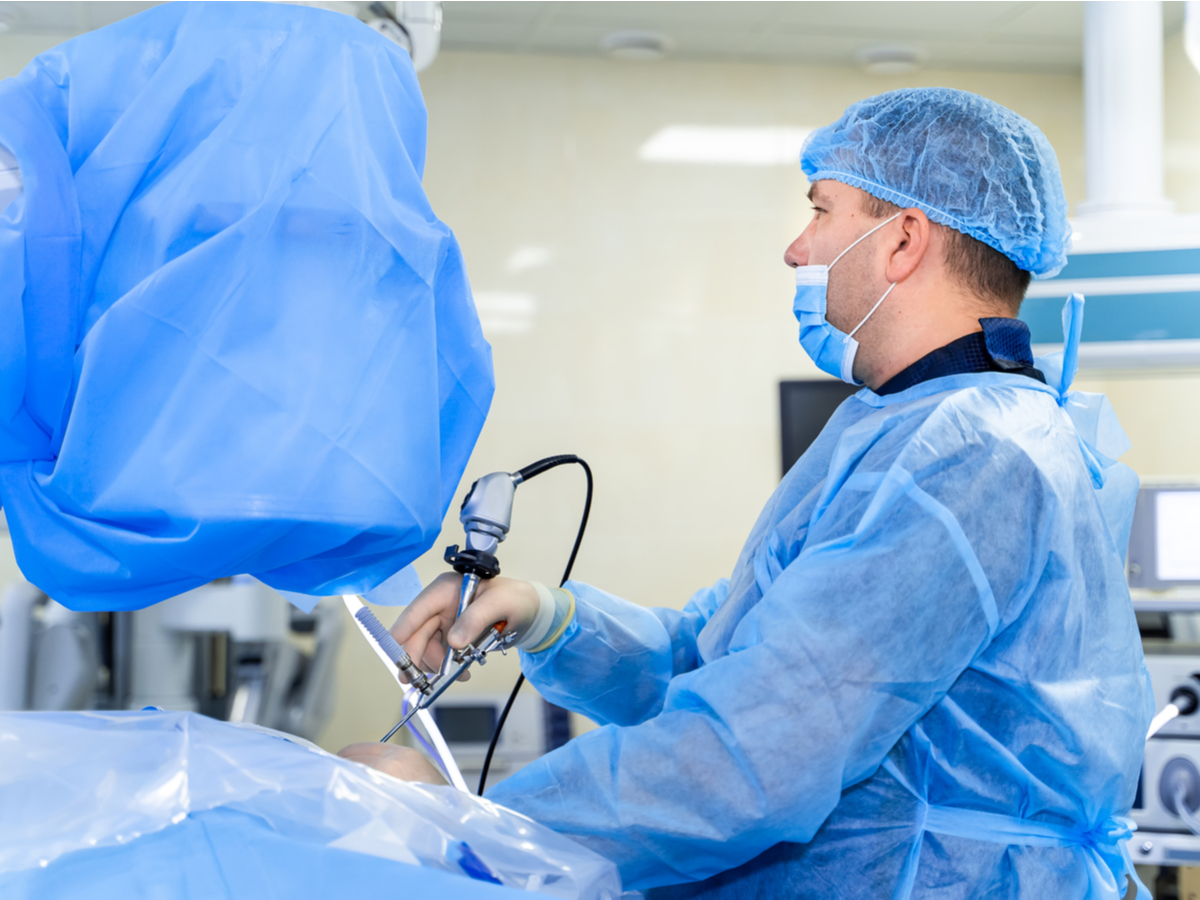





























Ihr Etikettierungssystem bei guter Gesundheit halten
Einhaltung von Vorschriften ermöglichen
Vereinfachen Sie die Compliance. Sie benötigen eine validierungsfähige Lösung mit integriertem rollenbasiertem Zugriff, Dokumentenversionierung, konfigurierbaren Genehmigungs-Workflows und elektronischen Aufzeichnungen und elektronischen Signaturen (ERES); die alle darauf ausgelegt sind, die Einhaltung von Vorschriften zu erleichtern.
Zuverlässige Datenquellen integrieren
Nutzen Sie sichere UDI-DI- und -PI-Daten. Vermeiden Sie unnötige Risiken, wenn Sie Daten aus zugelassenen Content-Management-Systemen, vertrauenswürdigen ERP-Systemen und anderen Anwendungen beziehen, die Seriennummern und andere Daten generieren, die für die Einhaltung gesetzlicher Vorschriften erforderlich sind.
Ihre Daten zentralisieren
Bieten Sie vollständige Transparenz. Ihr Unternehmen mag viele Standorte haben, aber das bedeutet nicht, dass jeder für sich selbst verantwortlich sein sollte. Eine zentralisierte Etikettierung bringt Transparenz und Kontrollen – und die Fähigkeit, Compliance zu demonstrieren und Unternehmensstandards zu erfüllen
Etikettenänderungen ermöglichen
Entlasten Sie die IT. Geschäftsanwender sollten in der Lage sein, medizinische Barcode-Etiketten zu erstellen und zu verwalten und Geschäftsregeln zu konfigurieren, ohne die IT-Abteilung einzuschalten. So können sie schnell auf alle dringenden Vorschriften reagieren.
Sicherheit/Auditierbarkeit gewährleisten
Sorgen Sie für sichere und zuverlässige Daten. Business Intelligence sowie umfassende Prüf- und Berichtsfunktionen ermöglichen Ihnen die Überwachung und Nachverfolgung aller Etikettierungsaktivitäten. eSignature-Funktionen sorgen zudem dafür, dass Sie Vorschriften sicher einhalten können.
Altsysteme überdenken
Automatisieren Sie für mehr Einfachheit. Tabellenkalkulationen und andere manuelle Prozesse sind nicht sicher. Mit automatisierten, validierten Etikettierungslösungen können Sie neue Anforderungen problemlos erfüllen, sich gegen künftige Vorschriften absichern und schnell skalieren.
Verwandte Ressourcen
E-Book
6 critical questions and answers on medical device labeling
This Q&A addresses key challenges that medical device companies face and how leveraging innovation in cloud labeling helps organizations succeed in a highly regulated, highly competitive global marketplace.
Webinar
2024 Top 5 Trends in Labeling and Packaging Artwork Webinar
Watch the Top 5 Trends in Labeling & Packaging Artwork webinar to explore supply chain complexity increases, how cloud becomes a cornerstone of digital transformation and more.
Bericht
Top-5-Trends 2024 für Etikettierung und Verpackungsdesign
Download this year’s Top 5 Trends in Labeling & Packaging Artwork report to discover why a commitment to bolstering digital transformation strategies through investment in innovative technologies will be critical to fortify supply chains against both current and future uncertainties. You’ll also find out how the supply chain continues to impact today’s businesses and why there is an increased focus on sustainability, digital traceability, automation, and more.